Пищевая аллергия
Содержание статьи
Пищевая аллергия – это одно из наиболее распространенных аллергических состояний, обусловленное непереносимостью соединений в составе некоторых продуктов питания. Проявления заболевания разнообразны: кожные симптомы (высыпания, зуд, крапивница), нарушения функции ЖКТ (диспепсические расстройства), иногда возможны системные анафилактические реакции. Диагностика производится посредством постановки кожных аллергологических проб, изучения анамнеза и пищевого дневника больного, выполнения лабораторных анализов. Лечение заключается в элиминации провоцирующих продуктов из рациона пациента, назначении антигистаминных средств, в редких случаях – десенсибилизирующей иммунотерапии.
Общие сведения
Пищевая аллергия является самой частой аллергопатологией, что обусловлено значительным разнообразием веществ, входящих в состав продуктов питания человека. Примерно половина больных – дети в возрасте до 12 лет, у старших лиц распространенность заболевания снижается. Более частое возникновение болезни у детей объясняется контактами с новыми для организма антигенами и повышенной реактивностью в данный период жизни. В дальнейшем на большинство соединений пищи вырабатывается иммунологическая толерантность, и проявления аллергии встречаются намного реже. Существует генетическая предрасположенность к развитию данного состояния, имеющая полигенный характер. В отдельных случаях непереносимость определенных продуктов сохраняется всю жизнь и может осложняться перекрестными реакциями и иными аллергическими состояниями (к примеру, бронхиальной астмой).
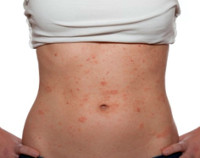
Пищевая аллергия
Причины
Большая часть случаев заболевания обусловлена гиперчувствительностью первого типа, опосредованной выделением IgE и активацией тканевых базофилов. Непосредственной причиной патологии является попадание в желудочно-кишечный тракт белковых соединений, которые распознаются иммунитетом и запускают его аномальный ответ. Выявлено огромное количество предрасполагающих к пищевой аллергии состояний и особенностей организма, часть которых характерна только для детей. Это является еще одной причиной частого развития аллергической реакции в детской популяции. Среди наиболее распространенных факторов, способствующих возникновению пищевой непереносимости, выделяют:
- Особенности аллергена. Гиперреактивность чаще вызывают антигены пищи, обладающие высокой иммуногенностью и способные без деградации преодолевать барьеры пищеварительной системы (в частности, агрессивную среду желудка). Большая часть из них содержится в коровьем молоке, рыбе, белке яиц, злаках, некоторых фруктах (клубника, цитрусовые) и орехах. Порядка 80% всех случаев заболевания обусловлено гиперчувствительностью к данным продуктам.
- Генетические факторы. Развитие непереносимости может быть обусловлено наследственными и генетическими свойствами организма. Они могут проявляться повышенным уровнем реактивности, аномальной активностью иммунитета и другими состояниями, облегчающими развитие аллергических реакций.
- Возрастные особенности ЖКТ. Возникновению аллергии на продукты способствуют наблюдаемая у детей высокая проницаемость стенок желудочно-кишечного тракта, низкая кислотность желудочного сока, нарушения состава микрофлоры кишечника. Эти условия облегчают контакт аллергена с иммунокомпетентными клетками, запускающими аллергический процесс.
На вероятность возникновения заболевания также влияет количество попавшего внутрь организма аллергена, характер кулинарной обработки продуктов, содержащих в себе провоцирующие вещества. Непереносимость продуктов может быть следствием перекрестной аллергии на пыльцу растений или бытовую пыль. Сенсибилизацию организма при этом вызывают антигены, переносимые по воздуху, но реакцию могут инициировать и продукты питания, имеющие схожие соединения в своем составе.
Патогенез
В процессе развития пищевой аллергии первоначально возникает сенсибилизация организма – она происходит при первом контакте с аллергеном. Последний распознается клетками иммунитета, которые через ряд промежуточных реакций вызывают образование иммуноглобулинов класса Е, специфичных к данному белковому соединению. Антитела такого типа обладают свойством адсорбироваться на поверхности тканевых базофилов, оставаясь там длительное время. При повторном поступлении провоцирующего антигена он связывается с IgE, которые активируют тучные клетки, вызывая их дегрануляцию с выходом гистамина. Этот биогенный амин обуславливает расширение кровеносных сосудов, отек тканей, раздражение нервных окончаний – данные изменения проявляются кожным зудом, крапивницей, диспепсическими расстройствами.
Особенностью аллергии к пищевым компонентам в младенческом возрасте является исключение этапа сенсибилизации из патогенетической цепи заболевания. Антитела против аллергена попадают в организм ребенка трансплацентарно или с грудным молоком от матери, которая страдает от непереносимости некоторых продуктов. По этой причине женщинам с аллергией особенно важно контролировать свое питание в период беременности и кормления грудью – в противном случае существует риск развития патологии у младенца. Но длительность такого состояния у детей незначительна – материнские антитела полностью элиминируются из организма через несколько недель после прекращения естественного вскармливания.
Симптомы пищевой аллергии
Клиническая картина патологии довольно разнообразна, статистически чаще регистрируются кожные симптомы, возникающие в течение 2-х часов после приема пищи. Развивается зуд, высыпания различной локализации, обычно эритематозного характера. Часть пациентов жалуется на крапивницу и иные отечные явления на поверхности кожи. В зависимости от тяжести аллергии и характера провоцирующего вещества эти симптомы могут сохраняться на протяжении нескольких часов или дней. После этого, при условии отсутствия контактов с аллергеном, кожные проявления обычно полностью и бесследно исчезают. При продолжении употребления опасного продукта аллергическая реакция регистрируется вновь, причем каждый новый эпизод характеризуется все более выраженными и тяжелыми симптомами.
Пищевая аллергия может проявляться нарушениями ЖКТ в первые часы после употребления аллергенных продуктов. Больные жалуются на боли в животе, тошноту, иногда рвоту и диарею. При особенно высокой аллергической готовности организма данные симптомы способны развиваться уже в момент приема пищи. Диспепсия сопровождается отеком слизистых оболочек полости рта, губ, поверхности языка. Иногда такой аллергический процесс приводит к заложенности носа, слезотечению, конъюнктивиту, что создает ложную картину поллиноза или непереносимости бытовой пыли.
Отдельные продукты питания (арахис, некоторые виды рыб, клубника) содержат аллергены, вызывающие сильные системные реакции – ангионевротический отек и анафилактический шок, сопровождающиеся спазмом гортани и падением артериального давления. У больных бронхиальной астмой гиперчувствительность к компонентам пищи может спровоцировать развитие приступа по механизму перекрестной аллергии. Ряд больных отмечает появление головных болей, повышенной утомляемости и слабости после употребления блюд с провоцирующими продуктами.
Осложнения
Наиболее тяжелым осложнением пищевой аллергии является анафилактический шок, вызванный массированной дегрануляцией базофилов и выделением большого количества гистамина. Он возникает при предрасположенности к непереносимости определенных продуктов или при длительном игнорировании проявлений заболевания. Продолжающееся поступление аллергена в организм приводит к постепенному нарастанию симптомов и в конечном итоге провоцирует развитие шока. Если аллергия сопровождается рвотой или диареей, то длительный контакт с антигеном может приводить к электролитным нарушениям. Среди других осложнений можно выделить возникновение перекрестной непереносимости антигенов цветочной пыльцы или бытовой пыли, инфицирование кожи в результате расчесов и повреждений.
Диагностика
Определение пищевой аллергии производится аллергологом-иммунологом, при этом важен тесный и доверительный контакт врача с пациентом или его родителями (при развитии патологии у детей). Для диагностики заболевания используют данные анамнеза, результаты лабораторных и иммунологических исследований, а также провокационных тестов. Последние следует использовать только в случае относительно низкой реактивности организма и легкости проявлений аллергии. При наличии риска системных реакций (отека Квинке или анафилактического шока) проведение исследований, предусматривающих контакт пациента с аллергеном, запрещено. Подтверждение диагноза и определение провоцирующего продукта проводят по следующему алгоритму:
- Осмотр и сбор анамнеза. Осматриваются кожные покровы больного для определения характера и выраженности высыпаний, в спорных случаях может потребоваться консультация дерматолога. Анализируется пищевой анамнез: выясняется, какие продукты употреблялись в последние дни и в каком количестве. На основе этого ограничивается круг возможных аллергенов, что облегчает дальнейшие исследования.
- Лабораторные анализы. В общем анализе крови незначительная эозинофилия определяется лишь при сильных либо неоднократных эпизодах аллергии. По показаниям микроскопическому исследованию подвергают смывы носоглотки, мазки-отпечатки с конъюнктивы – в них также обнаруживаются эозинофилы. Биохимическое исследование крови выявляет высокий уровень иммуноглобулинов классов E и G.
- Кожные аллергологические пробы. Для точного определения аллергена используют аппликационные пробы или прик-тест. При этом на кожные покровы наносят эталоны антигенов, попавших под подозрение в ходе расспроса больного. Развитие покраснения и отека является положительной реакцией и указывает на наличие непереносимости аллергена.
- Иммунологические анализы. К ним относят твердофазный иммуноферментный тест (ELISA) и радиоаллергосорбентный тест (RAST). Их проводят для определения типа провоцирующего антигена при высокой реактивности организма, когда кожные пробы исключены. Эти анализы с высокой точностью определяют наличие специфических к аллергену IgE в крови больного
Дифференциальную диагностику пищевой аллергии следует проводить с иными заболеваниями аллергического характера (поллиноз, атопический дерматит) и кожными патологиями (экзема, инфекционные поражения). При развитии диспепсических расстройств необходимо исключить риск пищевой токсикоинфекции или других болезней пищеварительной системы. Иногда симптомы, схожие с проявлениями аллергии, могут возникать из-за употребления непривычных или экзотических блюд. Обычно данные состояния самопроизвольно исчезают за несколько часов и редко возникают повторно.
Лечение пищевой аллергии
Лечебные мероприятия в практической аллергологии включают три этапа: облегчение симптомов аллергии, ускорение элиминации аллергена и предотвращение последующих контактов с ним. При непереносимости незаменимых продуктов питания используется десенсибилизирующая иммунотерапия. Важно также учитывать риск перекрестных реакций, поэтому после выявления аллергена специалист может ограничить потребление сразу ряда блюд. Их исключение из рациона надежно гарантирует отсутствие новых эпизодов пищевой аллергии. Основные этапы лечения складываются из:
- Симптоматической терапии. Применяют антигистаминные средства в различных формах выпуска – в виде таблеток, сиропов (в педиатрической практике) и назальных спреев. В большинстве случаев однократного приема препаратов данной группы достаточно для полного устранения проявлений пищевой аллергии. При более тяжелом течении специалистом может быть назначено их курсовое применение.
- Элиминации аллергена из организма. Может обеспечиваться как назначением специальной гипоаллергенной диеты, так и фармакологическими методами. В случае недавнего (несколько часов) попадания провоцирующего продукта в ЖКТ эффективны энтеросорбенты – активированный уголь, полисорб. Они связывают антигены в просвете кишечника, не позволяя им проникать в системный кровоток. Если после проникновения аллергенов прошло несколько дней, или они поступали в организм на протяжении длительного времени, то их элиминация возможна только естественным путем. Несколько ускорить ее можно инфузионной терапией или назначением диуретиков.
- Аллерген-специфической иммунотерапии (АСИТ). Этот этап лечения возможен только после полноценной диагностики патологии и точного определения провоцирующего антигена. Назначается в случае, если перечень запрещенных продуктов слишком обширен, или в него попадают незаменимые компоненты пищи. АСИТ заключается во введении постепенно повышающихся дозировок аллергена с целью выработки иммунологической толерантности к нему.
Прогноз и профилактика
Прогноз пищевой аллергии благоприятный, особенно при развитии состояния в детском возрасте – по мере роста ребенка непереносимость продуктов постепенно исчезает и практически не проявляется в дальнейшем. В случае наличия тяжелых реакций на арахис, морепродукты и некоторые фрукты довольно часто пациентам приходится пожизненно отказываться от их употребления. Кроме того, им рекомендуется иметь при себе средства для первой помощи при анафилактическом шоке (например, специальный шприц-ручку с адреналином). Профилактика сводится к ограничению использования продуктов высокого аллергического риска в детском питании и при беременности, а при наличии реакций – к их полному изъятию из рациона.
Источник
Иммунные реакции на пищу – пищевая аллергия разных типов – часть 2
Пищевая аллергия – это повышенный иммунный ответ на определенную пищу или пищевую добавку.
Особенности диагностики пищевой аллергии
Аллергия на пищевые компоненты может быть:
- IgE-зависимой – быстрый тип, тип I;
- независимой от IgE – медленный тип, что обычно означает реакции, индуцированные Т-лимфоцитами типа IV;
- смешанной.
Некоторые острые аллергические реакции на пищу могут привести к летальному исходу.
Диагностика пищевых аллергий сложна. Диагностировать аллергию на продукты помогает анамнез, лабораторные исследования, кожные аллергические пробы, элиминационная диета, исключающая аллерген, ПОМ (положительный провокационный пероральный тест). Образцы кожи и лабораторные анализы обычно только усиливают подозрение на аллергию.
Диагноз окончательно подтверждается или опровергается ПОМ. Для диагностики IgE-зависимой аллергии в сыворотке крови часто обнаруживают специфические антитела IgE к пищевым аллергенам. Количественные иммунные методы позволяют определять аллерген-специфические уровни IgE в сыворотке крови (МЕ/л) и класс (классы от I до VI).
Хотя диагноз пищевой аллергии окончательно подтверждается стандартизированным положительным провокационным пероральным тестом, ученые работают над установлением определенных диагностических пределов для конкретных антител IgE, чтобы избежать провокационных образцов. Это требует всесторонних исследований для установления диагностических пороговых значений для многих пищевых аллергенов.
Пищевая аллергия желудочно-кишечного тракта зависит от IgE
Большая поверхность слизистой оболочки кишечника постоянно подвергается воздействию посторонних веществ – от пищевых белков, естественной микрофлоры до болезнетворных микроорганизмов. Теоретически любой пищевой белок может сенсибилизировать организм и вызывать системные реакции быстрого типа.
Наиболее распространенные аллергены – водорастворимые гликопептиды.
- В 85% случаев ПА у детей вызывает коровье молоко (КМ), яйца, арахис, соевые бобы, орехи, рыба, моллюски и пшеница. Большинство детских аллергий развиваются с годами.
- Наиболее распространенные пищевые аллергены у взрослых – земля, фундук, грецкие орехи, фисташки, кешью, морепродукты.
![]() Пищевая аллергия желудочно-кишечного тракта зависит от IgE
Пищевая аллергия желудочно-кишечного тракта зависит от IgE
Симптомы ЖКТ обычно развиваются в период от нескольких минут до 2 часов после контакта с пищевым аллергеном. Симптомы ЖТ часто сочетаются с аллергическими симптомами других систем органов – кожи, дыхательных путей. Пациентов беспокоят тошнота, рвота, боли в животе. Брюшные колики обычно возникают через 1-2 часа, диарея – через 2-6 часов.
К врачу обычно больные обращаются по поводу плохого аппетита, плохого набора веса, периодических болей в животе. Часто с положительными кожными прик-тестами (ODM) на пищевые аллергены обнаруживаются в тестах повышенные уровни общего IgE и специфических антител IgE в сыворотке.
IgE-индуцированная локализованная пищевая аллергия называется синдромом оральной аллергии. Это форма контактной аллергии (эквивалент слизистой крапивницы), которая обычно поражает полость рта и горло. Основные аллергены – это фрукты и овощи – дыни, бананы, яблоки, киви, помидоры, лук-порей.
Клинические симптомы появляются очень быстро, часто во время еды, и длятся около 5-30 минут. Зуд губ, языка, неба, глотки, жжение, припухлость, покраснение, иногда зуд в ушах. Синдром оральной аллергии чаще всего встречается у подростков и взрослых с сезонным аллергическим ринитом, аллергией на пыльцу. Симптомы вызваны термостойкими аллергенами свежих фруктов и овощей, которые перекрестно реагируют с аллергенами пыльцы. Например, пациенты с аллергией на пыльцу березы.
Не-IgE-ассоциированная аллергия на пищу
Не-IgE-ассоциированная аллергия на пищу почти всегда возникает в первые месяцы жизни и редко выявляется у взрослых. Существует 3 основных клинических проявления не-IgE-ассоциированной ПА:
- энтероколит, индуцированный пищевым белком (MBSE);
- индуцированный пищевым белком проктоколит (MBSP);
- энтеропатия, индуцированная пищевым белком.
![]() Не-IgE-ассоциированная аллергия на пищу
Не-IgE-ассоциированная аллергия на пищу
Энтероколит (MBSE) – это атипичное редкое и трудно диагностируемое заболевание, характеризующееся повторяющимися эпизодами рвоты с диареей или без нее, которые проходят в течение 24 часов после отказа от диетического белка. Уровень заболеваемости MBSE составляет около 0,34%.
Точный механизм развития MBSE не ясен, но считается, что это реакция гиперчувствительности из-за клеточного иммунитета. Основные продукты, вызывающие энтероколит:
- коровье молоко;
- соя;
- рис.
Около трети пациентов с энтероколитом, вызванным молоком и соевым белком, страдают аллергией на зерно. Реже MBSE вызывается овсом и другими злаками, сладким картофелем, кабачками, морковью, яичным белком, фасолью, курицей, индейкой, рыбой и бананами.
Классические симптомы MBSE обычно возникают в течение первых 6 месяцев жизни (могут возникать до 1 года) и исчезают до 3 лет. Симптомы появляются в течение 1–4 недель после включения в пищу коровьего молока или соевого белка в рацион ребенка. Основные симптомы: периодическая обильная рвота (обычно через 2 часа) с диареей или без нее (через 2–10 часов, в среднем через 5 часов).
Иногда симптомы ухудшаются внезапно, с симптомами обезвоживания, гипотонии, летаргии или даже шока, как при сепсисе или остром животе, продолжительностью от 6 до 12 часов. Таким пациентам часто назначают лечение сепсиса, стеноза привратника или наследственного метаболического заболевания. Аллергическое происхождение симптомов даже не рассматривается, поскольку в крови обнаруживаются метаболический ацидоз, нейтрофилия и тромбоцитоз.
Около 30% больных с энтероколитом имеют другие аллергические заболевания, характерные для младенцев. Специфических диагностических образцов нет в 90% случаев. В некоторых случаях ODM дает отрицательный результат и пищевой специфический сывороточный IgE не выявляется.
Диагностировать MBSE у маленьких детей могут помочь образцы кожных пластырей. Но золотым стандартом в диагностике аллергического энтероколита считается положительный провокационный пероральный тест. Клинический диагноз обычно требует 6 эпизодов MBSE, поэтому диагностика может занять до 8 месяцев и более.
Проктоколит (MBSP ) – доброкачественное преходящее состояние у новорожденных, характеризующееся кровью и слизью в кале. Симптомы обычно возникают у ребенка в возрасте от 2 до 8 недель. При отсутствии системных симптомов, рвоты и нормальном росте ребенка заболевание нетрудно отличить от других симптомов ЖТ пищевой аллергии, проявляющихся колитом.
50-60% всех младенцев, страдающих этим заболеванием, находятся на грудном вскармливании, остальные получают коровье молоко или соевые смеси. Диагноз ставится при наличии свежей крови в фекалиях и отсутствии других системных симптомов. Симптомы исчезают после исключения молока из рациона кормящей матери и прекращения приема молочных детских смесей.
Энтеропатии, индуцированной пищевым белком, характеризуются длительной диареей, стеатореей, рвотой (60–70%), ранним чувством сытости и недостаточным набором веса в первые месяцы жизни. Иногда диагностируется анемия, гипопротеинемия. Потеря белка из-за энтеропатии может привести к отеку.
В большинстве случаев анализ крови на эозинофилию не показывает специфических антител IgE, общий уровень IgE в норме. Наиболее частая причина патологического состояния у младенцев – аллергия на белки коровьего молока. У детей старшего возраста – аллергия на сою, курицу, рыбу и рис. Эти пищевые аллергены вызывают клеточный иммунный ответ в тонком кишечнике, что приводит к неспецифической атрофии и лимфоцитарной инфильтрации.
Подобный патологический механизм существует и при целиакии, но дифференциальная диагностика не вызывает проблем, потому что энтеропатия, вызванная пищевым белком, начинается до отлучения от груди и без добавления глиадина в рацион. Диагноз ставится на основании клинических симптомов и их исчезновения после удаления аллергена. Во время ПОМ рвота и диарея возникают через 40-72 часа. Без пищевого аллергена симптомы исчезают в течение от 3 до 21 дня. Заболевание обычно длится не более 3 лет.
Комплекс IgE-зависимой и независимой пищевой аллергии
Примеры такой ПА – аллергия на белок коровьего молока (АБКМ), эозинофильный эзофагит (EE) и эозинофильный гастроэнтерит (EG). IgE-зависимые и IgE-независимые аллергические заболевания VT поражают детей всех возрастов как новорожденных, так и подростков.
АКПБ представляет собой аномальный ответ на белки молока, возникающий в результате иммунного ответа, вызываемого одним или несколькими белками. Это один из наиболее распространенных вариантов пищевой аллергии у младенцев и детей раннего возраста. Аллергия может быть вызвана прямым потреблением детских смесей с молоком и косвенно использованием молочных продуктов матерью во время грудного вскармливания.
Молоко – основной источник питательных веществ в течение первых 6 месяцев жизни. Поэтому большинство смесей для младенцев изготовлено из КМ, поэтому такая аллергия чаще всего диагностируется у детей, которые получают искусственное питание. АКПБ диагностируется примерно у 0,5% малышей на грудном вскармливании и у 2-5% малышей на искусственном вскармливании. Например, в Нидерландах около 7% детей обращаются к семейному врачу по поводу симптомов, связанных с применением молока.
Функциональные расстройства определяются как различные возрастные, хронические или повторяющиеся симптомы, которые нельзя объяснить структурными или биохимическими нарушениями.
![]() Комплекс IgE-зависимой и независимой пищевой аллергии
Комплекс IgE-зависимой и независимой пищевой аллергии
Аллергия на белок коровьего молока
Аллергия на белок коровьего молока может быть IgE-зависимой и независимой. Однако IgE, независимые от IgE реакции, встречаются реже.
- IgE-зависимая ПА проявляется, как и при большинстве других аллергий на IgE: крапивница, ангионевротический отек, рвота, диарея и анафилаксия (15% случаев). АБКМ также может вызывать респираторные симптомы, такие как хронический ринит или астма. Иногда являются единственными признаками являются раздражительность, головокружение и боль в животе.
- IgE-независимую АБКМ труднее идентифицировать. Обычно состояние проявляется устойчивым к лечению гастроэзофагеальным рефлюксом, экземой, постоянным плачем ребенка, диареей, а иногда и запорами. Эти симптомы трудно отнести к болезни, потому что они совпадают с обычными детскими недугами.
IgE-независимую АПФ следует подозревать у детей с атопическим дерматитом, если лечение ГЭРБ не удалось, симптомы проявляются более чем в одной системе органов, и наблюдается явный эффект от дозы коровьего молока. До 40%. ГЭРБ в детском возрасте может быть вызвана именно АБКМ.
Интерпретация симптомов ЖТ (срыгивание, рвота, гастроэзофагеальный рефлюкс, запор, диарея, колики у младенцев) очень сложна. Каждый из этих симптомов может возникать по ряду причин, но каждый также является симптомом IgE-независимой АБКМ.
Золотой диагностический стандарт для ПА и АБКМ – элиминационная диета и ПОМ: симптомы исчезают, если провокационная пища удаляется из рациона пациента, и симптомы повторяются, когда провокационный продукт возвращается в диету. Это исследование должно проводиться двойным слепым методом – ни пациент, ни врач, оценивающий исследование, не должны знать, является ли исследуемый продукт плацебо. К сожалению, положительные образцы не доказывают, были ли симптомы вызваны иммунным ответом. Реакции во время теста показывают только то, что симптомы провоцирует еда.
Для подтверждения диагноза аллергического заболевания необходимы доказательства того, что симптомы вызваны иммунологическими механизмами. Положительные специфические IgE, ODM или образцы кожи (OLM) и существующие симптомы, даже исключающие возможность ложноположительных тестов, подтверждают диагноз IgE-зависимого АБКМ.
В повседневной практике диагностические методы IgE-независимой диагностики отсутствуют. Провакационные пероральные тесты сложны в исполнении, они не демонстрируют точного механизма и не отвечают на вопрос, является ли это IgE-зависимой или независимой аллергией, или просто неиммунным ответом на коровье молоко. По этим причинам все эти условия сгруппированы вместе.
Аллерген-специфические тесты на IgE указывают на сенсибилизацию, а не на аллергическое заболевание. Чтобы продемонстрировать аллергию на белок коровьего молока, необходимо наличие истории быстрого ответа на молоко и положительного провокационного перорального теста. Если есть только симптомы, но нет сенсибилизации к IgE, нужно дифференцировать не-IgE-индуцированную АБКМ и неаллергическую чувствительность.
Ответ наступает в течение 2-6 недель. Аллергия подтверждается тем, что после непродолжительного возвращения к молоку симптомы возвращаются. Кормление грудью можно продолжить, если мать полностью откажется от молочного белка. Грудным детям назначают высокогидролизованные детские смеси. Они могут уменьшить регургитацию и гастроэзофагеальный рефлюкс за счет более быстрого опорожнения желудка.
Частично и сильно гидролизованные детские смеси уменьшают срыгивание, запор и боль в животе. Если они не помогают в течение нескольких недель, назначают смеси аминокислот. Некоторые пациенты склонны заменять молочные смеси на соевые или рисовые, но такие смеси подходят только в том случае, если запор спровоцирован именно коровьим молоком. Они не защищают от экземы или других проявлений пищевой аллергии, не относящихся к молоку, и поэтому не рекомендуются.
После подтверждения диагноза АБКМ положительным ПОМ, важно отличать симптомы аллергии на коровье молоко от функциональных симптомов ЖТ, связанных с пищевыми продуктами, поскольку долгосрочные последствия аллергии и функциональных симптомов ЖТ принципиально различаются. Раннее начало аллергического заболевания связано с двукратным повышением риска развития астмы и аллергического ринита в дальнейшем. До 90% детей с АКПБ начинают переносить молоко от коров в 3-летнем возрасте. Около 55% детей с IgE-зависимой АПФ начинают переносить молоко в возрасте 5 лет и 2,5 года – при не-IgE аллергии.
Функциональные симптомы ЖТ исчезают намного быстрее. Частота возникновения колик у младенцев снижается и полностью исчезает через 3–4 месяца, а рвоты – через 6 месяцев. Между тем функциональный запор не проходит спонтанно со временем. Таким образом, прогноз и отдаленный исход AM и функционального расстройства различны.
Как бы то ни было, совпадение симптомов ЖКТ при непереносимости белков АБКМ или молока и наиболее частых функциональных расстройств ЖТ, таких как гастроэзофагеальный рефлюкс и запор, было главной темой обсуждения в течение многих лет. Споры происходят из-за отсутствия объективных диагностических критериев для каждого из этих состояний. Нет единого специфического симптома непереносимости АКПБ или КП.
Для облегчения диагностики этих состояний в 2015 г. была опубликована специальная система оценки CoMiSS (оценка симптомов, связанных с коровьим молоком). Это только система рекомендательного характера (не диагностический тест на выявление аллергии), и она не заменяет провокационные пробы.
Аллергический эозинофильный эзофагит
Аллергический эозинофильный эзофагит – хроническое эозинофильное воспаление пищевода, которое встречается как у детей, так и у взрослых. Для патогенеза важны и пищевые, и вдыхаемые аллергены. Заболевание чаще всего диагностируется у 3-летних детей.
![]() Аллергический эозинофильный эзофагит
Аллергический эозинофильный эзофагит
Симптомы аллергического эозинофильного эзофагита аналогичны ГЭРБ: тошнота, рвота, рвота, боль в верхней части живота (груди), анорексия. Младенцы и маленькие дети беспокойны, плохо спят и худеют. Также могут возникать респираторные симптомы, такие как кашель и боль в груди. При длительном заболевании слизистая оболочка пищевода со временем сужается, что приводит к появлению у детей старшего возраста такого симптома, как нарушение (иногда болезненное) глотание твердой пищи.
Из-за неправильного диагноза дети нередко получают неэффективные антациды. Эндоскопически и гистологически характерный признак патологии – эозинофильное воспаление (≥15 эозинофилов в поле зрения при большом увеличении). 30-50% таких детей выявляются при бронхиальной астме, атопическом дерматите, аллергическом рините. У них часто бывает аллергия только на один пищевой аллерген.
Около половины пациентов имеют в крови эозинофилию. Уровень общего IgE в сыворотке нормальный или слегка повышенный. Недавние исследования показали, что могут помочь выявить пищевые аллергены комбинированные кожные инъекционные пробы и пластырь. Часто пациенты имеют в анамнезе ПА, положительный ODM и пищевой специфический IgE.
Наиболее распространенные пищевые аллергены, провоцирующие аллергический эозинофильный эзофагит, – молоко, соя, яйца и пшеница. Эффективные терапевтические методы лечения – местные кортикостероиды и эндоскопическое расширение стриктур пищевода, но не менее важно правильное питание. Относится к 6 продуктам элиминационной диеты – соя, пшеница, молоко, яйца, арахис, морепродукты.